Nous ne sommes pas des consultants, nous sommes des explorateurs

Notre vocation est d'explorer et développer les terres inconnues
En ce moment
Découvrez la Fondation Alcimed pour les maladies rares

Depuis plus de 30 ans
Notre équipe de 220 explorateurs accompagne nos clients à travers le monde dans leurs projets d’innovation et de développement de nouveaux marchés.
Notre aventureIls nous font confiance




















« Alcimed a la capacité de fournir des réponses venants des 4 coins du globe grâce à des équipes multiculturelles. »
Renaud JONQUIERES
Sr Vice President R&D Portfolio et Open Innovation


« Quand on définit une stratégie, on n'a pas toutes les réponses, ni même parfois pas toutes les questions ! »
Fabien DELAERE
Impact Valuation Directeur, Département Santé


« Nous recherchions un regard aiguisé qui nous permette de mieux analyser le marché sur des pays que l'on connaissait, ou au contraire des pays où l’on souhaitait s'implanter. »
Jérôme ARNAUDIS
VP Air Solutions
Nos missions
Nos expertises
Nos missions
Marketing stratégique
Clients & Patients
R&D
Stratégie commerciale
Innovation
Nouveaux partenaires
Nos expertises
Santé
Environnement & Climat
Beauté & Nutrition
Énergie & Mobilité
Souveraineté
Notre Journal de Bord
Santé
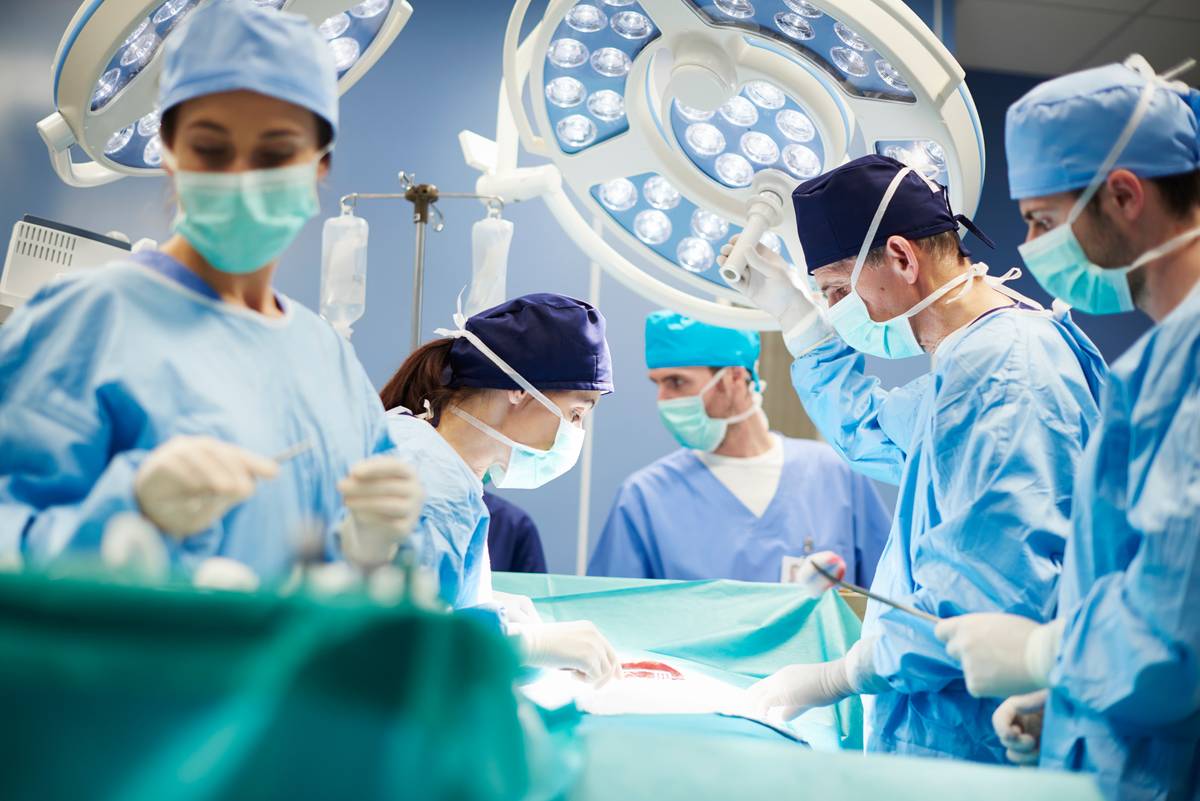
Enjeux et perspectives de la réhabilitation ex vivo des greffons pulmonaires
Qu’est-ce qu’une transplantation pulmonaire ? La transplantation pulmonaire est une intervention chirurgicale complexe visant à remplacer un poumon défaillant par un organe sain provenant ...
Santé
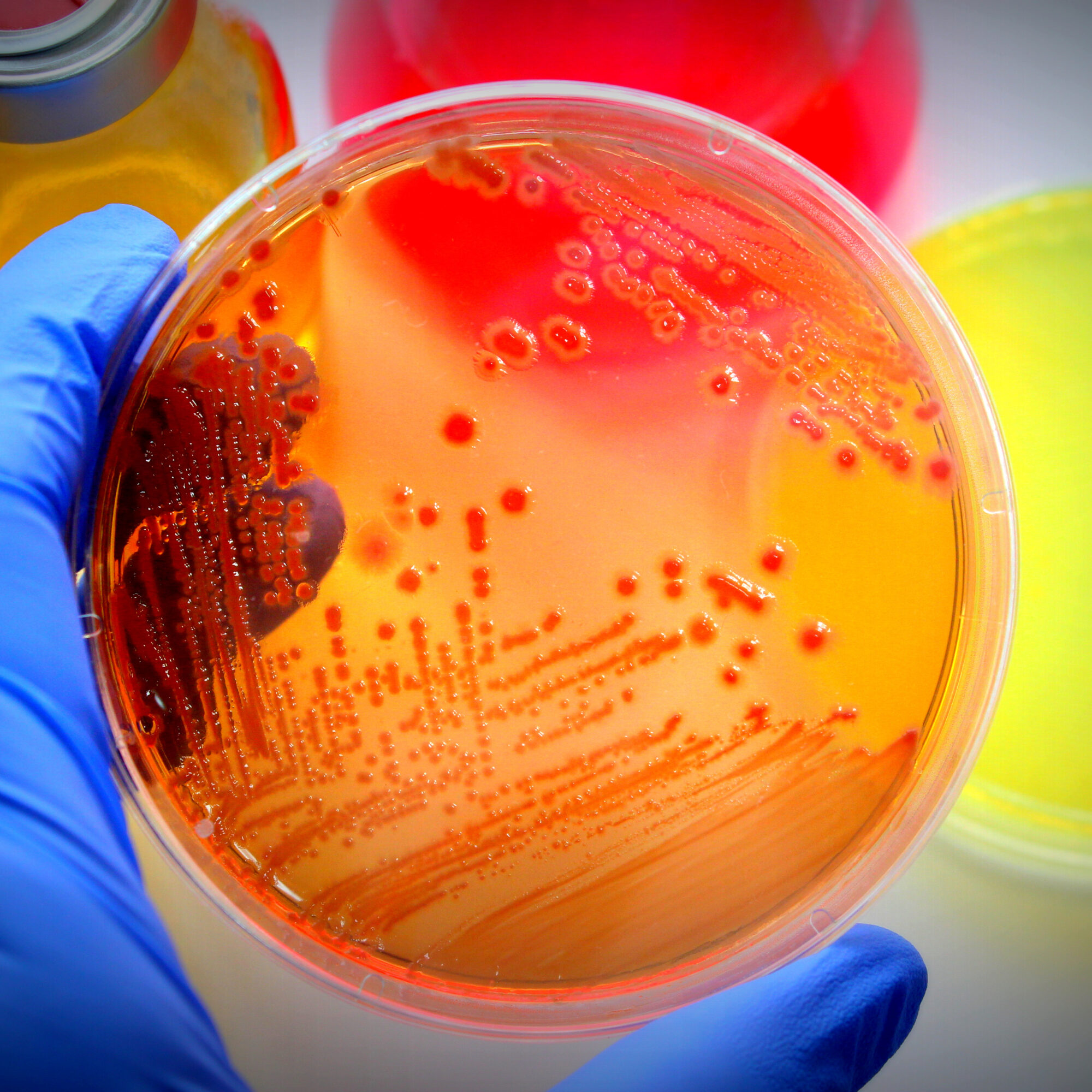
3 approches majeures à mettre en œuvre en R&D pour mettre fin à l’expérimentation animale dans l’industrie pharmaceutique
Approche n°1 : utilisation de technologies innovantes pour les essais in vitro Dans l'ère actuelle des progrès technologiques, des méthodes alternatives aux études sur les animaux sont ...
Santé
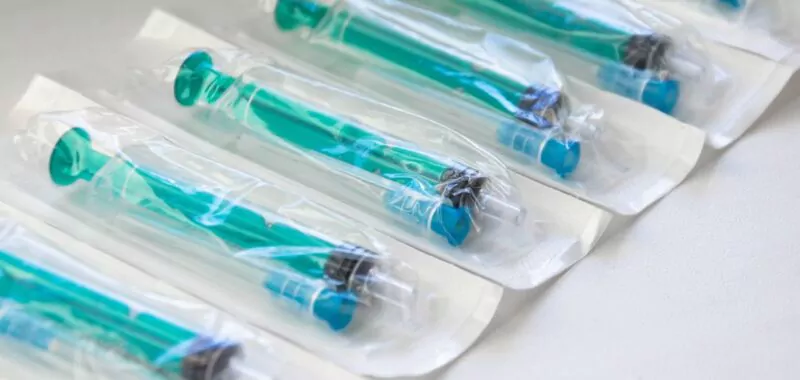
Comment relever le défi majeur du recyclage des seringues usagées ?
Les seringues usagées sont-elles recyclables ? Afin de créer une économie circulaire pour les seringues usagées, celles-ci doivent être fabriquées et consommées de manière à minimiser notre ...
Articles
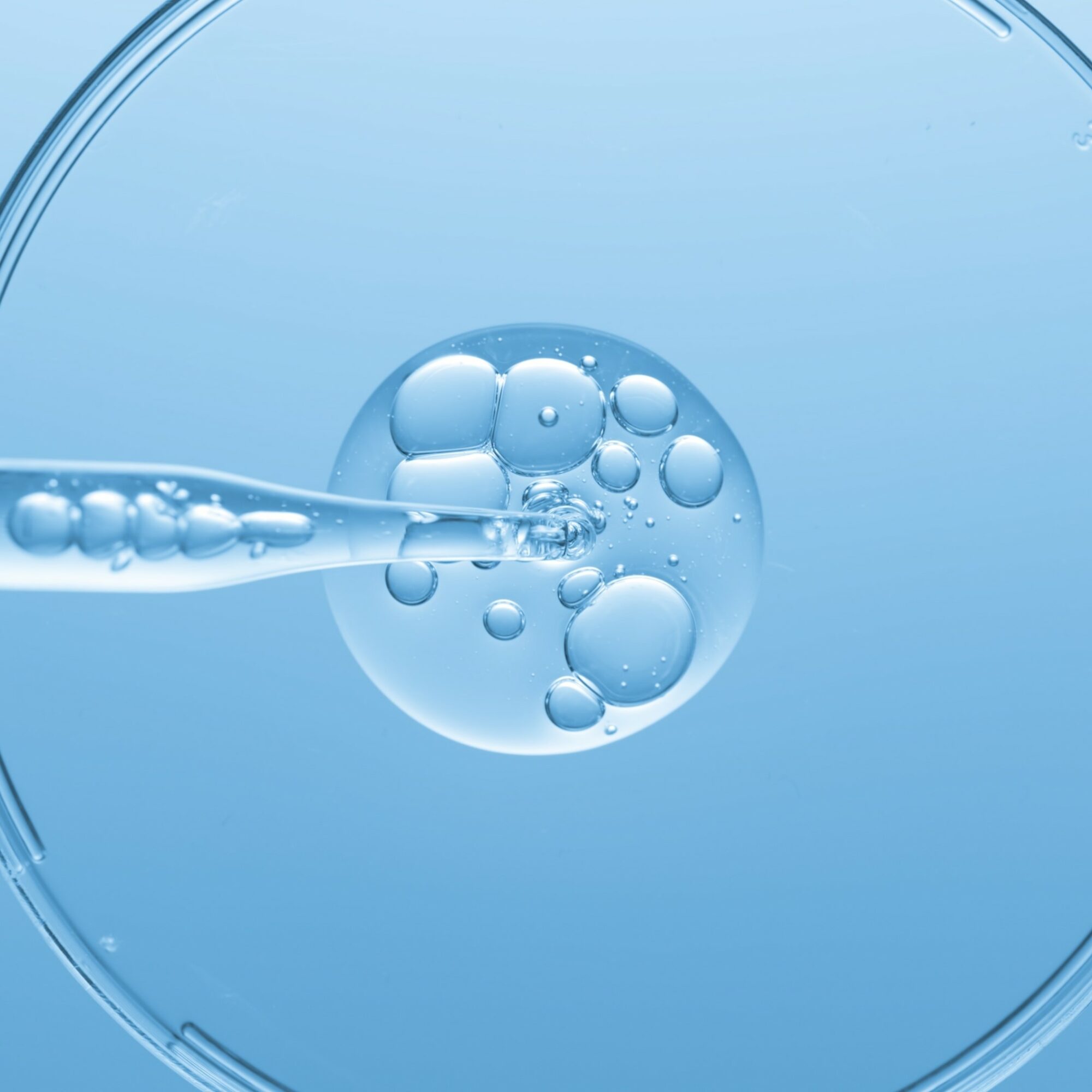
Quels enjeux pour le marché de l’acide hyaluronique en pleine expansion ?
Qu'est-ce que l'acide hyaluronique (AH) et comment est-il utilisé dans les procédures esthétiques ? L'acide hyaluronique est une molécule polysaccharidique et l'un des principaux composants du ...
Articles
Prise en charge de l’allergie : perspectives et enjeux de santé publique
Les allergies sont des pathologies bien connues et acceptées dans la population. A l’arrivée du printemps, de nombreuses personnes souffrent d’épisodes allergiques dus aux pollens. Si les ...
Découvrez nos articles et nos livres blancs sur notre Journal de Bord
Explorer notre Journal de Bord